金属が水や酸と反応するかどうかは、「イオン化傾向」によって決まります。
イオン化傾向が大きい金属は電子を放出しやすく、逆に小さい金属は安定しています。
本記事では、イオン化傾向の基本から順番の覚え方、実際の活用例までわかりやすく解説します。
試験対策や実生活にも役立つ知識を身につけましょう。
イオン化傾向とは?基本をわかりやすく解説
イオン化傾向とは、金属が電子を放出して陽イオンになりやすい度合いのことを指します。
イオン化傾向の一覧と定義、意味
金属によって電子を放出する(酸化される)しやすさには違いがあり、その順番を表したものが「イオン化傾向の一覧」です。

Li > K > Ca > Na > Mg > Al > Zn > Fe > Ni > Sn > Pb > (H) > Cu > Hg > Ag > Pt > Au
リチウム(Li)やカリウム(K)は非常にイオン化しやすく、空気中の水分とも反応して燃えてしまうくらいです。金属状態では安定しません。
逆に金(Au)はほとんどイオン化せず、安定した状態でいます。金は王水(濃硝酸と濃塩酸を3:1で混ぜたもの)にしか溶けないのは有名ですね。
これが「イオン化傾向が大きい・小さい」という概念です。
日常生活では、鉄が錆びやすいのに対し、装飾品としても人気のある金や白金はが錆びにくいのも、イオン化傾向の違いによるものです。
世界初のの電池であるボルタ電池やダニエル電池では、正極に銅(Cu)、負極に亜鉛(Zn)を使用しています。2つの電極のイオン化傾向の差が、電気を生み出す素となっています。
イオン化傾向の決まり方(電子との関係)
イオン化傾向は、金属原子が電子をどれだけ手放しやすいかで決まります。
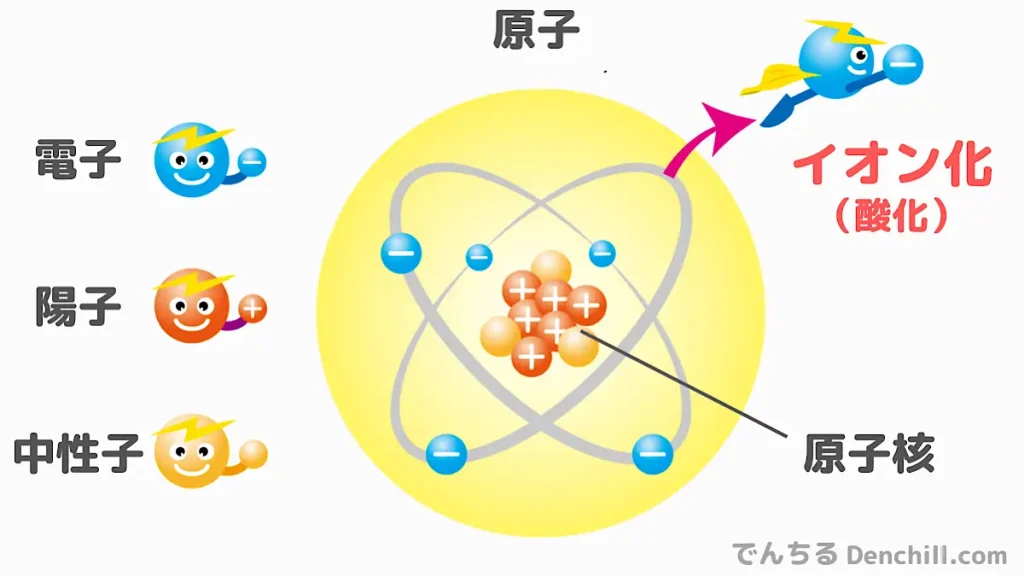
- 外側の電子が少ないほど手放しやすい
- 電子を手放すのにエネルギーが必要なものはイオン化しにくい
このため、周期表の左下にある金属ほどイオン化傾向が大きく、右上にある金属ほどイオン化傾向が小さい傾向にあります。
イオン化傾向が大きい・小さいとはどういうことか
イオン化傾向が大きい金属は、電子を放出しやすく酸化されやすいため、以下の特徴があります。
- 水や酸とよく反応する(例:ナトリウム、カルシウム)
- 腐食しやすい(錆びやすい)(例:鉄)
一方、イオン化傾向が小さい金属は、電子を手放しにくいため、安定している特徴があります。
- 水や酸と反応しにくい(例:銀、金)
- 装飾品や工業製品に利用される(例:金のアクセサリー)
イオン化傾向の順番と覚え方(語呂合わせ)
試験では、このイオン化傾向を暗記する必要があります。そこで、覚えやすい語呂合わせをお伝えします。
イオン化傾向の一覧と順番を再確認
代表的なイオン化傾向の順番は以下の通りです。
Li > K > Ca > Na > Mg > Al > Zn > Fe > Ni > Sn > Pb > (H) > Cu > Hg > Ag > Pt > Au
H(水素)より左側の金属は水素よりもイオン化しやすく、水や酸と反応しやすい金属です。
H(水素)よりイオン化傾向が小さい金属は、水や酸との反応性は落ちます。
イオン化傾向の語呂合わせを紹介(複数パターン)
イオン化傾向の順番は長くて覚えにくいため、語呂合わせがよく使われます。
- 1. 貸そうかな まあ あてにするな ひどすぎる 借金
-
- 貸そう:カリウム(K)
- か:カルシウム(Ca)
- な:ナトリウム(Na)
- ま:マグネシウム(Mg)
- あ:アルミニウム(Al)
- あ:亜鉛(Zn)
- て:鉄(Fe)
- に:ニッケル(Ni)
- する:スズ(Sn)
- な:鉛(Pb)
- ひ:水素(H)
- ど:銅(Cu)
- す:水銀(Hg)
- ぎる:銀(Ag)
- しゃっ:白金(Pt)
- きん:金(Au)
- 2. リッチに貸そうかな まああてにするな ひどすぎる借金
-
はじめに「リチウム(Li)」を追加
それぞれの元素記号を意識しながら、何度も口に出して覚えるのがコツです。
語呂合わせを使うことで、イオン化傾向の順番を短時間で覚えられます。ただし、試験では語呂合わせだけでなく、金属の性質とともに理解しておくことが大切です。
イオン化傾向と酸化・還元反応の関係
イオン化傾向と深い関わりのある、酸化還元反応との関係について解説します。
イオン化傾向と酸化・還元の基本原理
酸化・還元反応とは、電子をやりとりする化学反応のことです。
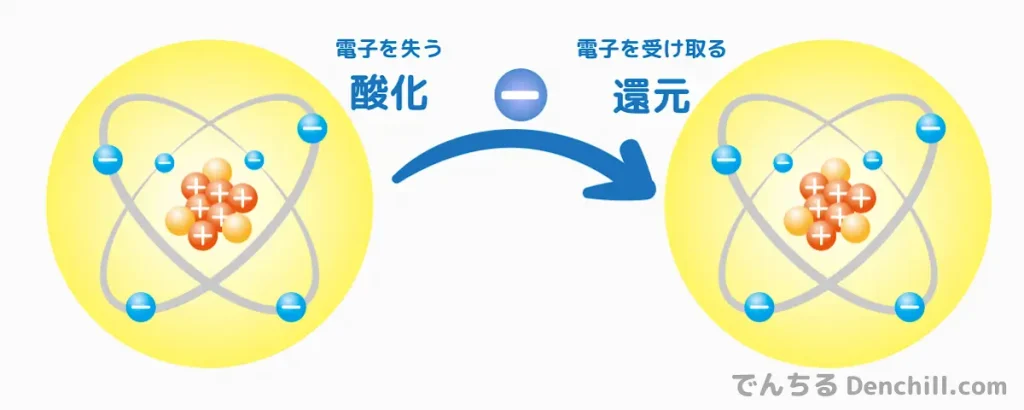
- 酸化:電子を失う(イオン化傾向が大きい金属ほど酸化されやすい)
- 還元:電子を受け取る(イオン化傾向が小さい金属ほど還元されやすい)
- イオン化傾向が大きいほど起こること(反応例)
-
イオン化傾向が大きい金属ほど、以下のような反応を起こします。
- 水と反応して水素を発生
(例:Na + H₂O → NaOH + H₂) - 酸と反応して水素を発生
(例:Zn + HCl → ZnCl₂ + H₂)
- 水と反応して水素を発生
逆に、イオン化傾向が小さい金属(Pt, Auなど)は酸と反応しにくく、安定しています。
- 金属のイオン化傾向と実生活での例
-
- 鉄が錆びやすいのは、酸素と反応して酸化鉄になるから
- 白金や金がアクセサリーに使われるのは、酸化されにくく美しいな状態を保ちやすい
イオン化傾向を理解することで、金属の特性を生かした製品選びや化学反応の応用ができます。
酸化反応と還元反応について詳しくは、
まとめ:イオン化傾向の覚え方と活用方法
イオン化傾向を理解することで、化学反応の予測や金属の特性を活かした活用が可能になります。
語呂合わせを活用しつつ、性質とセットで覚えることが重要です。

