電池は、内部で「酸化反応」と「還元反応」という化学反応を起こし、電子を移動させることで電気を発生させています。
本記事では、まず酸化還元反応の基本概念を解説し、次に乾電池や鉛蓄電池、リチウムイオン電池といった代表的な電池ごとの酸化還元反応の仕組みを詳しく紹介します。
酸化反応と還元反応とは?電池との関係
電池の仕組みを理解するうえで、まず「酸化反応」と「還元反応」について正しく理解することが重要です。
これらは「酸化還元反応」として対になって発生し、電池のエネルギー源となる反応です。
酸化還元反応の基本概念
酸化還元反応とは、物質が電子を失う「酸化」と、電子を受け取る「還元」が同時に起こる化学反応のことを指します。
- 酸化(Oxidation): 物質が電子を失うこと
- 還元(Reduction): 物質が電子を得ること
例えば、鉄(Fe)が空気中の酸素(O₂)と結びついて錆びる(酸化する)場合、以下のような反応が起こっています。
- 酸化反応:Fe → Fe3+ + 3e−
- 還元反応:O2 + 4e− → 2O2-
- 全反応:4Fe + 3O2 → 4Fe2O3
このように、電子を失う酸化反応と電子を受け取る還元反応は常に対になって進行します。これらをまとめて酸化還元反応といいます。
金属が酸化しやすいかどうかは「イオン化傾向」で表されます。
ここで注意が必要です。一般的に「酸化」と聞くと、酸素と結びつくことを指すと思われがちです。
しかし、酸化還元反応においては、「電子を失うこと=酸化」と言います。なので、酸素と結合する反応は酸化反応の中の1つですね。
ややこしいですが、覚えておいてください。
電子の移動と電気エネルギーの生成
電池が放電する時、その内部では負極(アノード)で酸化反応が、正極(カソード)で還元反応が発生します。
このとき、電子が外部回路を通って負極から正極へ移動することで電流が発生します。
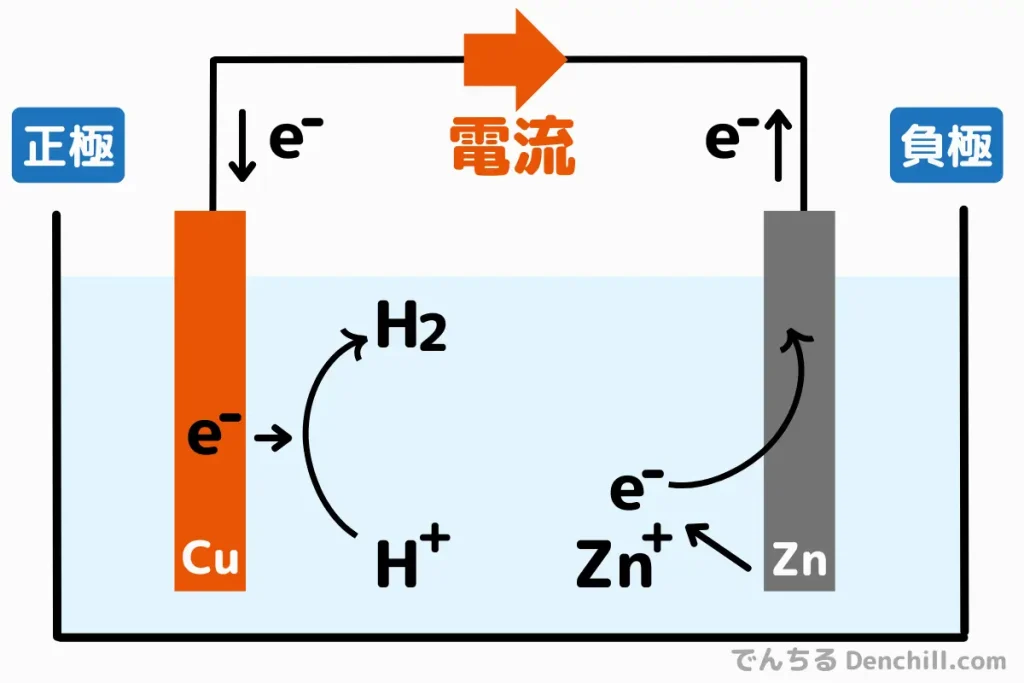
- 負極で酸化反応が起こる: 電極から電子が放出され、イオンが溶液中に溶ける。
- 外部回路を通じて電子が流れる: 電気エネルギーとして利用される。
- 正極で還元反応が起こる: 電子を受け取ったイオンが安定した物質へ変化する。
※実際は全てが同時に起こります
この電子の流れが電池から電流が流れ、電力を生み出す仕組みです。
電流の流れる向きは電子の流れる向きと反対なので注意してください。
酸化剤と還元剤の役割
電池の化学反応には「酸化剤」と「還元剤」が重要な役割を果たします。
- 酸化剤(Oxidizing agent):他の物質を酸化させ、自分は還元される物質(例:酸素、二酸化マンガン)。
- 還元剤(Reducing agent):他の物質を還元させ、自分は酸化される物質(例:亜鉛、リチウム)。
電池では、これらの物質の組み合わせによって、安定した電気エネルギーを取り出せるよう設計されています。
電池ごとの酸化還元反応の具体例
ここでは、代表的な電池の種類ごとに、具体的な酸化還元反応を詳しく見ていきます。
乾電池の化学反応(マンガン乾電池・アルカリ乾電池)
乾電池は一次電池(充電不可)であり、マンガン乾電池とアルカリ乾電池が代表的です。
- 正極(還元反応):MnO2 + H+ + e- → MnO(OH)
- 負極(酸化反応):Zn → Zn2+ + 2e-
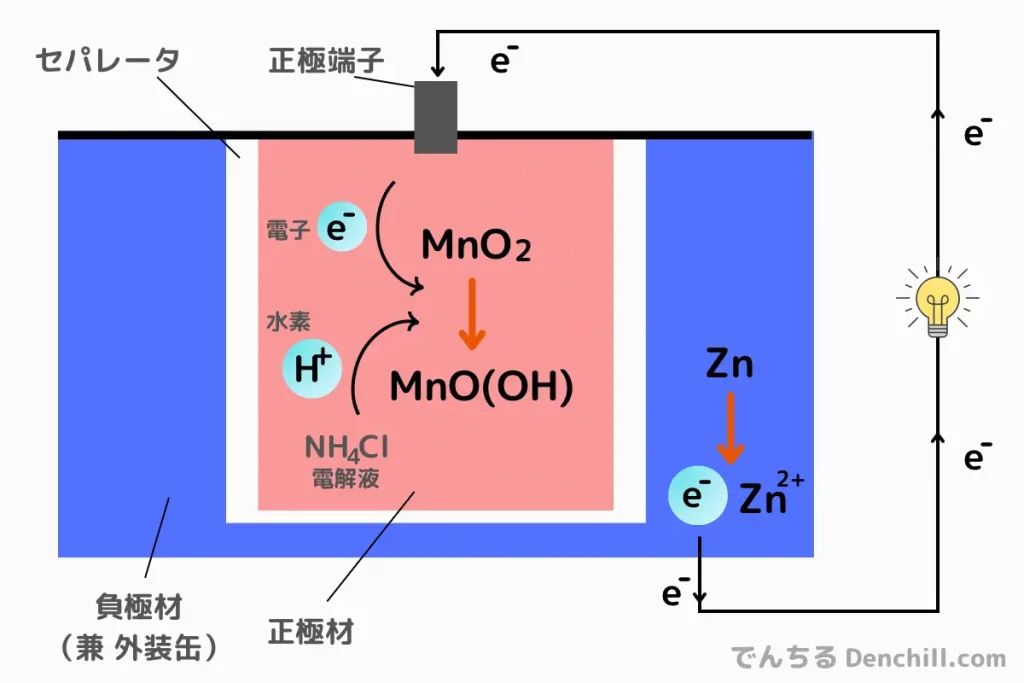
正極では酸化マンガンがこの反応により電子が流れ、電流が発生します。
鉛蓄電池の酸化還元反応と特性
鉛蓄電池は、自動車のバッテリーとして使われる二次電池(充電可能な電池)です。
- 正極(二酸化鉛の還元):PbO2 + SO42− + 4H+ + 2e− → PbSO4 + 2H2O
- 負極(鉛の酸化):Pb + SO42−− → PbSO4 + 2e−
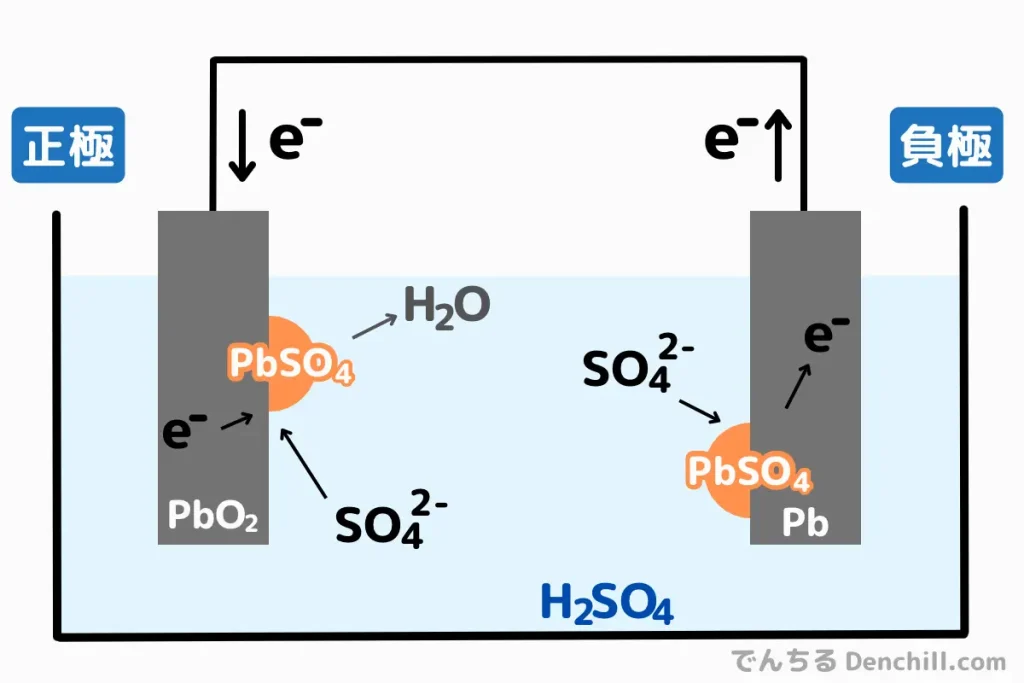
充電時には逆の反応が起こり、再び鉛と二酸化鉛に戻ります。
リチウムイオン電池の酸化還元反応と充放電の仕組み
リチウムイオン電池はスマートフォンや電気自動車に使用される高性能な二次電池です。
- 正極(コバルト酸リチウムの還元):
xLi+ + Li1-xCoO2+ xe− → LiCoO2 - 負極(リチウムの酸化):
LiC6 → xLi+ + Li1-xC6 + xe−
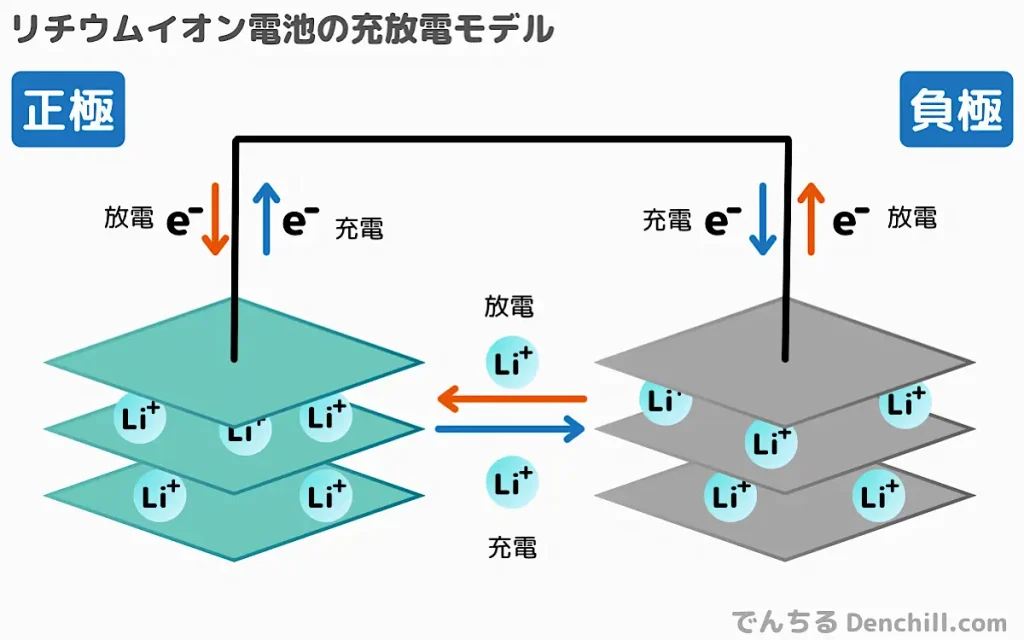
リチウムイオン電池は、正極はコバルト酸リチウムが、負極では炭素が層状の構造をしています。
その層の間を、充電と放電時にリチウムイオンが移動します。
それにより、エネルギーを貯めたり放出したりします。
まとめ – 酸化還元反応は充電放電の基本
電池は、酸化還元反応によって電子を負極から正極に移動させることで電流を生み出します。
乾電池、鉛蓄電池、リチウムイオン電池など、種類ごとに異なる化学反応が用いられています。
共通しているのは「電子の流れを利用してエネルギーを取り出す」という点です。
このシンプルな原則を理解することで、電池のことをもっと理解できるようになるでしょう。

