電池は現代の生活に欠かせない存在ですが、その歴史は18世紀末に発明された「ボルタ電池」にさかのぼります。
ボルタ電池には”分極”という欠点があり、改良されたものが「ダニエル電池」です。
これらの電池は、学校の理科や化学の授業でも学ぶ重要なテーマです。
本記事では、ボルタ電池とダニエル電池の原理や仕組み、特徴、そして両者の違いについて詳しく解説します。
ボルタ電池とは?その仕組みと特徴
ボルタ電池は、世界で初めて実用化された電池です。1800年にイタリアの科学者アレッサンドロ・ボルタによって発明されました。
正極と負極で起こる酸化還元反応を利用した化学電池の元祖ですね。
ボルタ電池の基本原理と構造
ボルタ電池の基本構造は以下の通りです。
- 構成材料
-
- 亜鉛板(負極)
- 銅板(正極)
- 酸性または塩基性の電解液(硫酸・塩酸など)
- 仕組み
-
- 亜鉛(Zn)は電子を放出し、酸化反応を起こす。
- 放出された電子が外部回路を通って銅電極に流れる。
- 銅電極では、電極上で水素イオン(H+)が電子を受け取り還元反応を起こし、水素ガス(H2)として放出される。
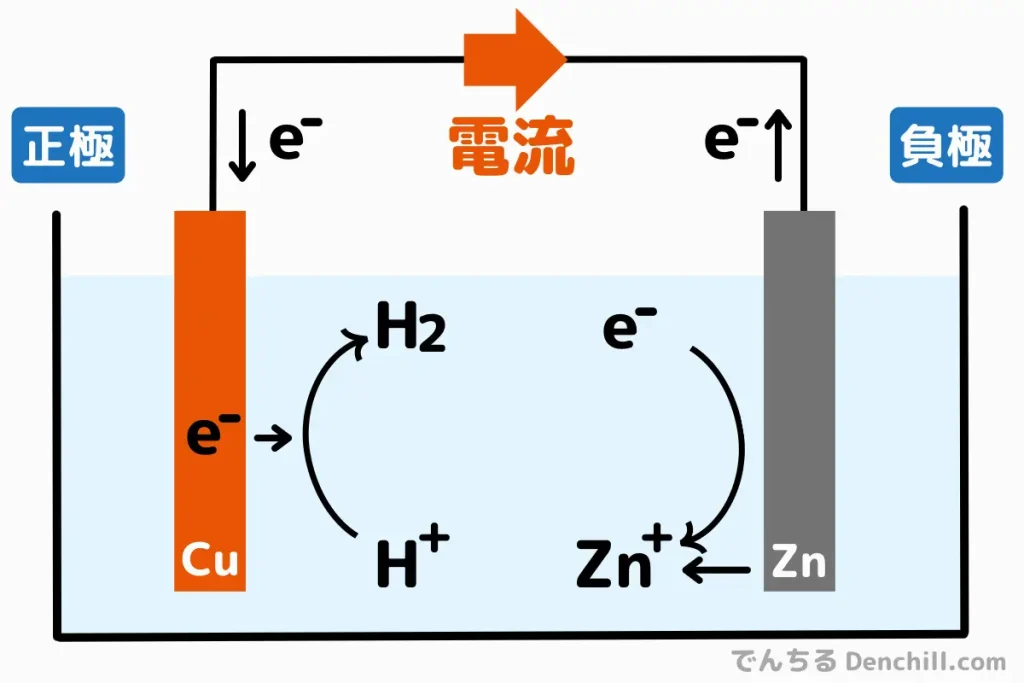
ボルタ電池は単純な構造で電気を発生させることができます。
ボルタ電池の化学反応式
ボルタ電池の化学反応を以下に示します。
- 化学反応式
-
- 正極(還元反応):2H+ + 2e- → H2
- 負極(酸化反応):Zn → Zn2+ + 2e-
- 全体の反応式:Zn + 2H+ → Zn2+ + H2
この反応によって電子が流れ、電流が発生します。しかし、この構造には大きな欠点がありました。
ボルタ電池の課題「分極」
ボルタ電池を放電していると、電池の起電力が低下してきます。これが「分極」という現象です。
分極は電池の正極で水素ガスが発生し、その水素が電極を覆うことで電流の流れが妨げられる現象を指します。
この水素の層が電子の流れを妨げるため、時間が経つと発電しにくくなります。
この分極問題を解決するために改良されたのが、次に紹介するダニエル電池です。
ボルタ電池に関するよくある間違いと正しい理解
ボルタ電池について、以下のような誤解が多くあります。
ボルタ電池は長時間使える?
いいえ、分極の影響で短時間で電圧が低下します。
ボルタ電池は乾電池のように使える?
強い酸を使うため、取り扱いが難しく、実用的ではありません。
ボルタ電池はすぐに発電する?
はい、電極と電解液を用意すれば、すぐに電流が流れます。
ダニエル電池とは?ボルタ電池との違いを解説
ボルタ電池の欠点を解決するために、1836年にイギリスの化学者ジョン・ダニエルが考案したのがダニエル電池です。
ダニエル電池は、分極を防ぐために硫酸銅溶液を使用し、長時間安定した電流を流せるように改良されました。
ダニエル電池の原理と仕組み
ダニエル電池の基本構造は以下の通りです。
- ダニエル電池の構成
-
- 負極:亜鉛板
- 正極:銅板
- 負極側電解液:液硫酸亜鉛溶液
- 正極側電解液:硫酸銅溶液
- 隔膜:半透膜または塩橋
- 化学反応式
-
- 正極(還元反応): Cu2+ + 2e- → Cu
- 負極(酸化反応): Zn → Zn2+ + 2e-
- 全反応式:Zn + Cu2+ → Zn2+ + Cu
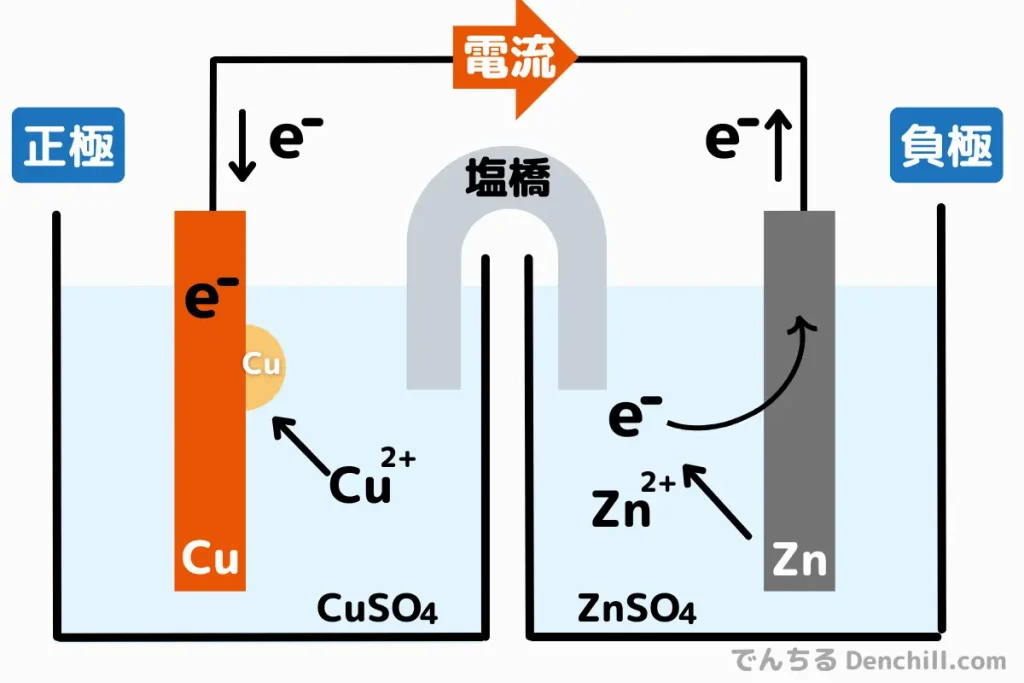
正極と負極を分離し、硫酸から硫酸銅水溶液に変更しました。銅は水素よりもイオン化傾向が小さいので、水素発生せずにドアの析出反応が起こります。
これで正極を分極が防がれ、安定した電流を供給できるようになります。
この構成でダニエル電池はボルタ電池と同じように電子が流れ、電流が発生します。
しかし、ボルタ電池と異なり、正極側の銅電極には水素ガスが発生しないため、分極の影響を受けにくいという特徴があります。
ボルタ電池とダニエル電池の比較
ボルタ電池とダニエル電池の違いを表にまとめます。
| 項目 | ボルタ電池 | ダニエル電池 |
|---|---|---|
| 発明者 | アレッサンドロ・ボルタ(1800年) | ジョン・ダニエル(1836年) |
| 負極 | 亜鉛(Zn) | 亜鉛(Zn) |
| 正極 | 銅(Cu) | 銅(Cu) |
| 電解液 | 酸(塩酸や硫酸など) | 硫酸亜鉛 硫酸銅溶液 |
| 欠点 | 分極が起こる(水素ガスが電極に付着) | 分極が起こらない |
| 電圧 | 約0.76V | 約1.1V |
| 持続性 | 短時間しか使えない | 長時間安定した電流を供給できる |
- 分極の防止:硫酸銅溶液を利用することで、水素ガスの発生を抑制。
- 安定した電流の供給:電池の寿命が長く、安定して電力を供給可能。
- 高い電圧:ボルタ電池よりも高い電圧(約1.1V)を発生できる。
このように、ダニエル電池はボルタ電池の問題点を解決し、電池技術の発展に大きく貢献しました。
実験で確かめる!ボルタ電池とダニエル電池の発電の仕組み【小学生・中学生向け】
ボルタ電池やダニエル電池は、簡単な材料で再現できます。例えば、以下のような方法で実験が可能です。
特にボルタ電池については、100均の材料でも簡単にできるので、実験にはおすすめです。
ボルタ電池の実験
- 材料
-
- 亜鉛板
- 銅板
- 希硫酸(バッテリー液など)
- 導線
- 電球やモーター
- 手順
-
- 食塩水に亜鉛板と銅板を入れる。
- 導線でつなぐと、電球がわずかに点灯する。
希硫酸はホームセンター等の車用バッテリーのコーナーに行けば、バッテリー液として購入できます。
ただ、実際にこの実験を行うと、亜鉛からもガンガン気泡が出ます。これは、亜鉛が硫酸に溶けてしまうからです(Zn + 2H+ → Zn2+ + H2)。なので、ボルタ電池の実用性の無さがよく分かると思います。
とはいえ、こちらの実験はかなり手軽におこなうことができます。レモン電池は希硫酸をレモンの果肉に置き換えたものです。
ダニエル電池の実験
- 材料
-
- 亜鉛板
- 銅板
- 硫酸亜鉛溶液
- 硫酸銅溶液
- 塩橋
- 導線
- 電球やモーター
- 手順
-
- 硫酸亜鉛水溶液に亜鉛板、硫酸銅水溶液に銅板を浸す。
- 2つの溶液を塩橋で繋ぐ
- 導線を接続すると電球が光る。
硫酸亜鉛や硫酸銅はAmazonなどで購入可能です(まあまあな値段しますが)。
塩橋は本来であれば電解質を含んだゼラチンや寒天などを用いますが、電解液で湿らせたティッシュなどでも代用可能です。
また、これらは化学薬品を使用しますので、安全性や廃棄方法は事前に確認しておきましょう。
これらの実験を通じて、電池の仕組みを実際に体験してみましょう。
まとめ
ボルタ電池とダニエル電池は、電池技術の基礎を築いた重要な発明です。
- ボルタ電池:世界初の電池だが、分極の問題がある。
- ダニエル電池:ボルタ電池の改良版で、分極が起こらず長時間使用できる。
- どちらも電池技術の発展に大きく貢献し、現代の乾電池やリチウムイオン電池につながっている。
この知識を活かし、電池の仕組みを深く理解していきましょう!

